- Роль генетического профилирования опухоли: как современные технологии помогают в борьбе с раком
- Что такое генетическое профилирование опухоли?
- Как проводят генетическое профилирование?
- Преимущества и ограничения генетического профилирования
- Практические примеры использования генетического профилирования в онкологии
- Что дальше? Перспективы развития генетического профилирования
Роль генетического профилирования опухоли: как современные технологии помогают в борьбе с раком
Когда мы думаем о борьбе с онкологическими заболеваниями‚ часто представляем себе хирургические операции‚ химиотерапию или облучение․ Однако за кулисами борьбы с раком происходят удивительные и сложные процессы‚ которые меняют подход к лечению практически с каждым годом․ Одним из ключевых направлений в современном онкологии становится генетическое профилирование опухоли․ Этот метод позволяет выявлять уникальные особенности каждой опухоли на молекулярном уровне‚ что открывает новые горизонты для индивидуализированного подхода к лечению․
В этой статье мы подробно расскажем о роли генетического профилирования в современной медицине‚ о том‚ какие возможности оно предоставляет‚ и как помогает врачам разрабатывать наиболее эффективные тактики борьбы с злокачественными образованиями․ Мы обсудим‚ каким образом генетические исследования меняют представление о диагнозе‚ прогнозе и терапии‚ а также расскажем о конкретных примерах успешных применений этого метода․
Что такое генетическое профилирование опухоли?
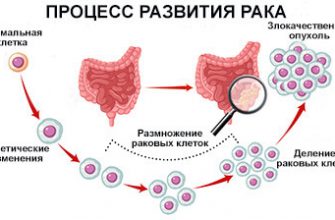
Генетическое профилирование опухоли — это процесс изучения её молекулярной генетической информации с целью выявления изменений (мутаций‚ амплификаций‚ делециий и других аномалий)‚ характерных для конкретного ракового образца․ Благодаря современным методам секвенирования и анализа данных‚ исследователи получают подробное «меню» генетических особенностей опухоли‚ что позволяет понять её поведение‚ устойчивость к терапии и потенциальную чувствительность к лекарственным препаратам․
Этот подход коренным образом отличается от классических методов диагностики‚ которые основаны на гистологическом исследовании клетки и микроскопическом наблюдении․ Генетическое профилирование дает более глубокое понимание молекулярных механизмов развития заболевания и механизмов его сопротивляемости лечению․
| Особенности | Описание |
|---|---|
| Индивидуализация терапии | Позволяет выбрать лекарства‚ наиболее подходящие для конкретного генетического профиля опухоли․ |
| Прогнозирование | Помогает определить вероятность рецидива‚ прогрессирования или ответной реакции на лечение․ |
| Обнаружение мишеней | Находит молекулярные мишени для таргетной терапии и иммунотерапии․ |
| Контроль эффективности | Используется для отслеживания генетических изменений в опухоли во время лечения․ |
Как проводят генетическое профилирование?
Процесс начинается с взятия образца опухолевой ткани — часто это материал‚ полученный при хирургическом или биопсийном вмешательстве․ Современные лабораторные методы позволяют проводить молекулярный анализ даже на очень небольшом объеме материала․ В дальнейшем образец подвергается различным видам секвенирования — наиболее распространенным является следующее поколение секвенирования (NGS)‚ которое позволяет быстро и очень точно определить массив генетических изменений․
Главные этапы процесса:
- Образец и подготовка: сбор и подготовка образца ткани․
- Извлечение ДНК: получение идеального образца для анализа․
- Генетическое секвенирование: использование технологий‚ таких как NGS․
- Анализ данных: обработка и интерпретация результатов на компьютере․
- Интерпретация и отчет: подготовка документа для врача и пациента․
Полученные результаты позволяют выявить мутации и генетические аномалии‚ которые в дальнейшем станут основой для выбора индивидуальной терапии․ Важно отметить‚ что современные лаборатории используют специализированное программное обеспечение‚ позволяющее определить значимость найденных изменений и рекомендации по дальнейшему лечению․
Преимущества и ограничения генетического профилирования
Преимущества этого подхода очевидны:
- Персонализированное лечение: возможности подобрать наиболее эффективные препараты․
- Повышение шансов на выздоровление: за счет более точных и целевых методов терапии․
- Избежание ненужных побочных эффектов: исключение неэффективных методов․
- Прогнозирование риска: выявление вероятности рецидива и метастазирования․
Однако‚ есть и ограничения:
- Высокая стоимость исследований и необходимости современных лабораторий․
- Не все мутации можно интерпретировать однозначно‚ что может влиять на выбор терапии․
- Генетическая изменчивость опухоли: в процессе лечения могут возникать новые аномалии‚ меняющие профиль опухоли․
Кроме того‚ не все виды опухолей хорошо поддаются генетическому анализу‚ и иногда требуется сочетание методов для максимально точной оценки состояния пациента․
Практические примеры использования генетического профилирования в онкологии
Рассмотрим несколько ярких случаев‚ когда генетическое профилирование сыграло решающую роль в определении тактики лечения:
| Тип рака | Ключевые гены и мутации | Выход из ситуации |
|---|---|---|
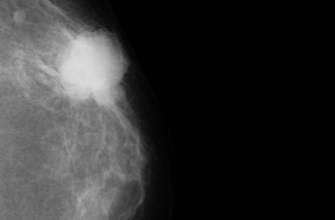
| Рак молочной железы | BRCA1‚ BRCA2 | Выбор таргетных препаратов PARP-ингибиторов и иммунотерапии․ |
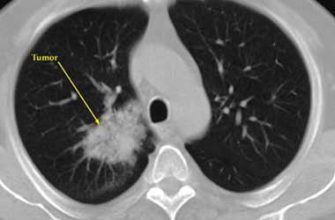
| Нехорошо поддающийся лечению рак легких | EGFR‚ ALK | Назначение тирозинкиназных ингибиторов и иммунотерапии․ |
| Общий саркома | Мутации в TP53‚ KIT | Выбор химиотерапии и таргетных лекарств․ |
Такие примеры показывают‚ как молекулярные особенности позволяют не только ставить точный диагноз‚ но и максимально эффективно использовать возможности современной медицины․
Что дальше? Перспективы развития генетического профилирования
Будущее онкологии — это‚ безусловно‚ развитие методов персонализированной медицины․ Сегодня ученые работают над созданием огромных баз данных с генетическими профилями множества типов опухолей‚ что позволяет разрабатывать новые препараты и комбинации лекарств․ Также активно внедряются новые технологии‚ такие как жидкостная биопсия‚ которая позволяет получать необходимую информацию о генетическом профиле опухоли без необходимости операции или биопсии ткани․
Следующие шаги включают использование искусственного интеллекта и машинного обучения для автоматической интерпретации генетических данных‚ что повысит точность и скорость диагностики․ В перспективе возможно создание персональных профилей всего организма на молекулярном уровне‚ что сделает лечение практически максимально точечным и эффективным․
Подробнее
| генетическое тестирование опухоли | персонализированная терапия рака | молекулярный профиль опухоли | NGS в онкологии | таргетная терапия рака |
| гены при раке молочной железы | иммунотерапия и генетика | жидкая биопсия | искусственный интеллект в онкологии | мутации и лечение рака |